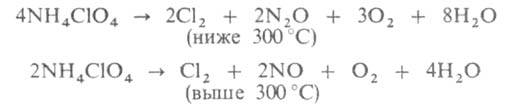Химическая энциклопедия
"АММОНИЯ ПЕРХЛОРАТ"
Главная - Химическая энциклопедия - буква А - АММОНИЯ ПЕРХЛОРАТ
АММОНИЯ ПЕРХЛОРАТ
NH4C1O4, бесцв. кристаллы;
ниже 238°С устойчива ромбич. модификация (а = 0,9225 нм, в = 0,5815 нм,
с = 0,7456 нм, z = 4, пространств. группа Ршш); плотн. 1,952 г/см3;
Соp 128,1 Дж/(моль*К); Выше 150°С А. п. заметно разлагается (см. ур-ния ниже), выше 250 °С
он также возгоняется с диссоциацией на NH3 и НСlO4
(при 270°С давление диссоциации ~ 13 Па). В интервале 150-300°С изотермич.
разложение А. п. идет автокаталитически и практически прекращается после
распада ок. 30% в-ва. Остаток по составу и св-вам практически не отличается
от исходного А. п., но имеет цеолитоподобную структуру. Способность вновь
подвергаться такому распаду возвращается к остатку после обработки его
парами в-в, растворяющих А. п., или после перекристаллизации. Распад А.
п. выше 300°С идет до конца и не автокаталитически. Кубич. модификация
немного стабильнее ромбической, поэтому в области т-р фазового перехода
(235-250°С) скорость распада уменьшается с ростом т-ры. Обработка А. п.
парами НС1О4 ускоряет разложение, парами NH3-замедляет.
Состав продуктов распада приближенно м. б. выражен ур-ниями:
В пром-сти А. п. получают обменной р-цией NaClO4 с NH4C1, (NH4)2SO4 или (NH4)2CO3, а также взаимод. водных р-ров НС1О4 с NH3. Применяют А. п. как окислитель твердых ракетных топлив и смесевых ВВ. А. п. взрывоопасен, чувствителен к удару, трению, огню. Объем произ-ва в США 50 тыс. т/год (1969). Лит.: Механизм, кинетика и катализ термического разложения и
горения перхлората аммония, пер. с англ., Новосиб., 1970.
|
Поделитесь с друзьями:
Вы можете поставить ссылку на это слово:
будет выглядеть так: АММОНИЯ ПЕРХЛОРАТ
будет выглядеть так: Что такое АММОНИЯ ПЕРХЛОРАТ
 Нообр- 295,2 кДж/моль; выше 238°С устойчива кубич.
форма (а = 0,763 нм, пространств. группа Fm3m), плотн. 1,732 г/см3
при 270°С;
Нообр- 295,2 кДж/моль; выше 238°С устойчива кубич.
форма (а = 0,763 нм, пространств. группа Fm3m), плотн. 1,732 г/см3
при 270°С;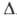 H°
полиморфного перехода 9 кДж/моль. С повьпиением давления т-ра перехода
растет, достигая 300°С при 0,4 ГПа. Р-римость А.п. при 25°С (г в 100 г
р-рителя): в воде - 24,92; метаноле - 6,85; этаноле - 1,90; ацетоне - 2,26.
А. п. раств. в расплаве LiClO4, эвтектика NН4СlO4
- LiClO4 имеет т. пл. 182°С и содержит 32,6% А. п.
H°
полиморфного перехода 9 кДж/моль. С повьпиением давления т-ра перехода
растет, достигая 300°С при 0,4 ГПа. Р-римость А.п. при 25°С (г в 100 г
р-рителя): в воде - 24,92; метаноле - 6,85; этаноле - 1,90; ацетоне - 2,26.
А. п. раств. в расплаве LiClO4, эвтектика NН4СlO4
- LiClO4 имеет т. пл. 182°С и содержит 32,6% А. п.