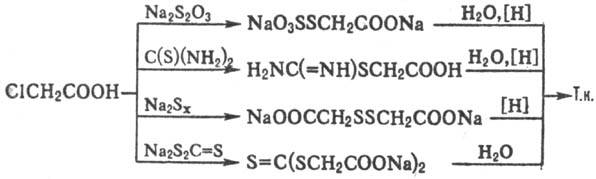Химическая энциклопедия
"ТИОГЛИКОЛЕВАЯ КИСЛОТА"
Главная - Химическая энциклопедия - буква Т - ТИОГЛИКОЛЕВАЯ КИСЛОТА
ТИОГЛИКОЛЕВАЯ КИСЛОТА
(меркаптоуксусная к-та) HSCH2COOH, мол. м. 92,11; бесцв. жидкость
с сильным неприятным запахом; т. пл. — 16,5°С, т. кип. 123°С/29 мм рт.
ст., 90°С/6 мм рт. ст.; В водных р-рах с концентрацией
ниже 70% Т. к. стабильна при 20 °С, в более конц. р-рах и при повыш. т-ре
происходит самоэтерификация с образованием S-меркаптоацетилтио-уксусной к-ты
HSCH2qO)SCH2COOH, циклич. 1,4-дитио-гликолида и политиогликолидов. Для Т.к. характерны св-ва
карбоновых кислот
и тиолов
(образование солей, сложных эфиров,
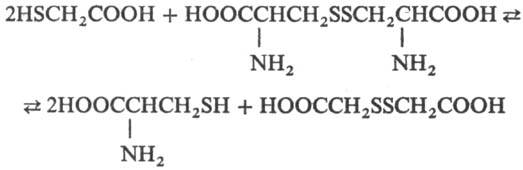
амидов, тиолятов, сульфидов, дисульфидов). Обратимо взаимод. с дисульфидами,
напр. цистином (скорость, при к-рой устанавливается равновесие, мала при рН
< 6 и велика при рН На этой р-ции основано
использование Т. к. для хим. завивки волос (производные Т. к.-аммониевая соль,
соль моно-этаноламина, моноглицериновый эфир-разрушают связи S—S цистина в кератине
волос, под действием окислителей эти связи снова образуются). Т.к. легко окисляется (особенно
в щелочных р-рах) в присут. солей Сu, Мn или Fe до дитиодигликолевой к-ты
(HOOCCH2S)2 либо ее солей; сильные окислители (напр.,
разб. HNO3) превращают Т.к. в сульфоуксусную к-ту HSO3CH2COOH. Т. к. замещает атом H
тиольной группы в р-циях с алкил-галогенидами, алкилендигалогенидами, хлоруксусной
к-той, ацетилхлоридом в присут. щелочей; присоединяется к непредельным соед.;
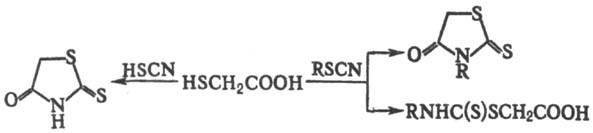
с альдегидами и кетонами (при соотношении 1:2) образует тиоацетали RRC(SCH2COOH)2. Взаимодействие Т.к. с тиоциановой
к-той приводит к 2-тионо-1,3-тиазолидин-4-ону (роданину); с N-замещенными изотиоцианатами
при рН 3,0-7,5-к N-замещенным родани-нам, при рН>9,5-к N-замещенным тиокарбамоилтио-гликолевойк-ты:
Получают Т. к. обработкой
К- или Na-соли хлоруксусной к-ты гидросульфидами щелочных металлов в водной
среде; побочно образуются гликолевая, тио- и дитиодигликолевые к-ты. Во избежание
образования побочных продуктов м.б. использованы др. соединения S, напр. Na2S2O3,
полисульфиды щелочных металлов, тиомочевина, тритиокарбонат Na, напр.: Для качеств. определения
Т.к. используют нитропруссид Na в аммиачном р-ре, образующий с Т.к. фиолетово-пурпурную
окраску, для количественного-иодометрич. титрование. Композиции эфиров Т.к.
и оловоорг. соединений применяют для стабилизации ПВХ, тиогликоляты используют
в качестве добавок, регулирующих мол. массу продуктов полимеризации акрилонитрила
и метилметакрилата. Т.к. применяют также как добавку к фиксирующим р-рам в фотографии
для предотвращения выделения серебра на стенках ванн, при травлении для снижения
коррозии металла, для растворения и удаления лигнина из древесины, что обусловлено
способностью Т. к. расщеплять полифенольные материалы, напр. таннины и лигнин.
В сочетании с красителями, реагирующими с группами HS, Т. к. применяют для окраски
волос, кремы на основе Na- или Са-солей Т. к. с рН 10,0-12,5 используют в качестве
депиляторов. Т. воспл. > 110°С,
ПДК 0,1 мг/м3, ЛД50 250-300 мг/кг (мыши, перорально) и
120-150 мг/кг (крысы, перорально). Лит.: Kirk-Othmer
encyclopedia, 3 ed, v. 22, N. Y., 1983, r. 933-46. А. А. Дудинов. |
Поделитесь с друзьями:
Вы можете поставить ссылку на это слово:
будет выглядеть так: ТИОГЛИКОЛЕВАЯ КИСЛОТА
будет выглядеть так: Что такое ТИОГЛИКОЛЕВАЯ КИСЛОТА
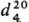 1,3253;
1,3253; 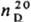 1,5030;
1,5030;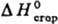 - 1446 кДж/моль; pKa1
3,55-3,92, рКа2 9,20-10,56. Смешивается
во всех соотношениях с водой, метанолом, этанолом, ацетоном, диэтиловым эфиром,
хлороформом, бензолом. Практически не раств. в алифатич. углеводородах.
- 1446 кДж/моль; pKa1
3,55-3,92, рКа2 9,20-10,56. Смешивается
во всех соотношениях с водой, метанолом, этанолом, ацетоном, диэтиловым эфиром,
хлороформом, бензолом. Практически не раств. в алифатич. углеводородах.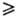 8
— 10):
8
— 10):