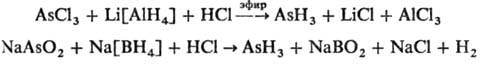Химическая энциклопедия
"МЫШЬЯКА ГИДРИД"
Главная - Химическая энциклопедия - буква М - МЫШЬЯКА ГИДРИД
МЫШЬЯКА ГИДРИД
(арсин,
мышьяковистый водород) AsH3, газ без цвета и запаха (но часто имеет
чесночный запах, обусловленный продуктами частичного окисления М.г.). Молекула
пирамидальная с атомом As в вершине; углы HAsH 92,08°, длина связи AsH 0,1511
нм. Т.пл. — 117°С,
т.кип. — 62,5 °С; плотн. газа 3,5 г/л, жидкого -1,766 г/см3 при
-111,8 °С и 1,64 г/см3 при -64,3°С; С0Р
38,7Дж/(моль.К); DH0пл 1,2 кДж/моль,
DH0исп 16,7 кДж/моль, DH0обр
— 66,4 кДж/моль; S0298 223,0 ДжДмолъ.К);
ур-ния температурной зависимости: давления пара (мм рт.ст.) над твердым в-вом
lgp = 6265,9 Т-1 — 260,99 + + 98,51 lg 74 39,6.10-3
T (141,6-159,8К), над жидкостью lgp = 6640,56T-1
- 388,57 + 171,53 lg Т-183.39•10-3 Т (166,5—210,7
К), вязкости h = 0,4984.10-7T1,015 Па.с
(213-273 К). Р-римость при 25 °С (см3/см3): в воде-0,28,
ацетоне-9,3, хлороформе-10,9, нитробензоле-11,72, вазелиновом масле-22,7. М.г. медленно разлагается
на элементы уже при комнатной т-ре, быстро и нацело-ок. 500 °С. Термич.
разложение М.г. с осаждением As на горячей пов-сти в виде зеркала используют
для обнаружения As даже в очень малых кол-вах (проба Марша). При обычной т-ре
М.г. не окисляется О2. С хлором взаимод. с воспламенением уже при
— 196 °С, с Вг2 и I2-при комнатной т-ре с образованием
соответствующих галогенидов As. С серой дает H2S и As. С сухим НСl
и разб. соляной к-той не реагирует, с конц. соляной к-той дает AsCl3
и Н2, с конц. H2SO4-As и высшие арсины. Окислители
в водных р-рах окисляют М.г. до As2O3, в р-рах солей Ni
и Со образуются арсениды этих металлов. При нагр. нек-рых металлов с М.г. получают
арсениды. Щелочные металлы в аммиачном р-ре образуют с М.г. металл-арсины, напр.
NaAsH2 и Na2AsH. Выделены также аммиакаты, напр. NaAsH2.2NH3
и LiAsH2.4NH3. Металларсины с СН3Сl
дают моно- и диметиларсины. Получают AsH3
кислым гидролизом арсенидов Mg, Zn и др., восстановлением соед. As водородом,
взаимод. галогенидов As или др. соед. As с Li[AlH4], Na[BH4]
или др. гидридами, напр.: Применяют AsH3
для легирования полупроводниковых материалов мышьяком, для получения As высокой
чистоты. Токсичен; ПДК 0,0003 мг/л.
Отравление возможно при травлении к-тами металлов, содержащих даже малую примесь
As. М.г. легко воспламеняется. Известны неустойчивые высшие
арсины: диарсин As2H4, разлагается уже при —100 °С,
образуется при взаимод. AsCl3 с Li[AlH4]; т р и а р с
и н As3H5. Предполагают существование твердых гидридов
AsHx (0,5 < х < 1). При действии тихого электрич. разряда
на смесь AsH3 с SiH4 или GeH4 получают гидриды
составов SiAsH5, SiAsH7 или GeAsH5. Об алкил-
и ариларсинах см. в ст. Мышьякорганические соединения
. А. И. Горбунов, П. А.
Стороженхо. |
Поделитесь с друзьями:
Вы можете поставить ссылку на это слово:
будет выглядеть так: МЫШЬЯКА ГИДРИД
будет выглядеть так: Что такое МЫШЬЯКА ГИДРИД