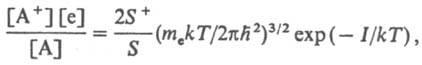ИОНЫ В ГАЗАХ
, образуются в заметных концентрациях при высоких т-рах, а также при воздействии на газ фотонами или быстрыми частицами. Играют существенную, а зачастую и определяющую роль в радиац. химии, плазмохимии, лазерной химии, физико-химии верх. слоев атмосферы, межпланетного пространства и космоса, а также в ядерной технике и в условиях мощного энергетич. воздействия.
Элементарные процессы образования И. в г. Взаимод. нейтральных частиц с потоком быстрых электронов (электронный удар) приводит к образованию положит. ионов, если энергия электронов Ее равна или превышает потенциал ионизации I нейтральной частицы А (атома,
молекулы): А + е : А+ + 2е. При Ее>1 с ростом Ее вероятность процесса растет вначале линейно, достигает максимума в области значений Ее, соответствующих 3-5 I, а затем плавно уменьшается. В максимуме сечение ионизации si, определяемое как эффективная площадь поперечного сечения нейтральной i-й частицы, в к-рое должен попасть электрон, чтобы произошла ионизация, составляет обычно 0,2-0,5 от газокинетич. сечения, т.е. определяется фактически геом. размерами ионизуемых частиц. При дальнейшем увеличении Ее различия в величине si для разных атомов и молекул сглаживаются, и при достаточно больших значениях Ее величина si определяется гл. обр. числом электронов в ионизируемой частице. Зная si, можно рассчитать кол-во ионов Ni, образующихся в слое газа толщиной d в единицу времени при прохождении через него потока электронов Ne. Для "оптически тонкого" слоя, когда длина своб. пробега электронов в газе dn >> d, Ni = sindNe, где п - концентрация ионизируемых частиц.
При взаимод. электронов с молекулами наряду с образованием мол. ионов возможна и диссоциативная ионизация с образованием осколочных ионов, напр.: Н2 + е : Н+ + Н + 2е. Такой процесс становится возможным, когда Ее достигает нек-рой пороговой величины. В приведенном примере эта величина (потенциал появления иона Н+) равна сумме потенциала ионизации атома Н I(Н) = 13,6 эВ и энергии диссоциации D(H-H) = 4,5 эВ и составляет 18,1 эВ. Однако поскольку, согласно принципу Франка - Кондона, с наиб. вероятностью происходят вертикальные квантовые переходы, при к-рых не изменяется расстояние между атомами в молекуле, энергия, необходимая для диссоциативной ионизации, часто оказывается больше пороговой величины. Так, для образования Н и Н+ из низшего колебат. уровня основного электронного состояния 1Sд Н2 необходимо возбудить молекулу в состояние 2Sи, энергия к-рого превышает порог ионизации на 10-14 эВ (см. рис.).
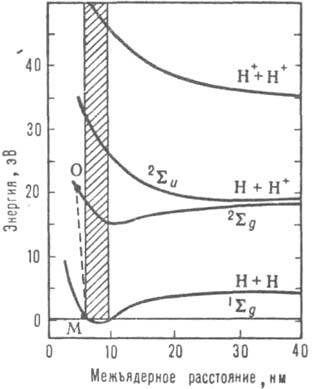
Рис. 1. Кривые потенциальной энергии молекулы Н2. Заштрихованной полосой показаны границы вертикальных (франк-кондоновских) переходов из основного состояния 1Sд в возбужденные 2Sд и 2Sи. Пунктирная линия МО - невертикальный переход.
Избыточная энергия переходит в кинетич. энергию частиц Н и Н+ . Существенно меньше вероятность "невертикального" перехода в состояние 2Sд, приводящего к образованию медленных частиц. Т. обр., при диссоциативной ионизации электронным ударом возможно образование "горячих" частиц, чего не происходит при образовании атомарных и мол. ионов.
При диссоциативной ионизации многоатомных молекул избыточная энергия перераспределяется по степеням свободы таким образом, что разрыв хим. связи происходит по наиб. слабой из них и положит. заряд оказывается, как правило, у осколка с наим. потенциалом ионизации.
При столкновении электронов с атомами и молекулами возможно образование не только положительных, но и отрицат. ионов. Для этого необходимо, чтобы частицы обладали положит. сродством к электрону и чтобы избыток энергии, возникающий в частице после захвата электрона, был отдан системе прежде, чем произойдет диссоциация на электрон и исходную частицу. При прилипании электрона к
атому избыточная энергия, равная сумме кинетич. энергии электрона и сродства атома к электрону, м. б. испущена в виде кванта света (радиац. процесс) либо передана при столкновении третьей частице (или пов-сти). Вероятность Wr радиац. процесса типа А + е : А- + hn (n - частота испускаемого кванта света, h - постоянная Планка) при энергии Ее ~ 10 эВ равна ~ 10-7 и изменяется в первом приближении пропорционально 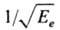 . Вероятность Wt передачи энергии возбуждения третьей частице пропорциональна концентрации таких частиц и зависит от их природы. Во всех случаях сечение прилипания электрона к атомам существенно меньше газокинетич. сечения, в отличие от сечений ионизации при образовании положит. И. в г.
Существенно большими сечениями обладают процессы образования отрицат. ионов многоатомных частиц. Это объясняется тем, что возбужденная многоатомная частица может быстро диссоциировать: . Вероятность Wt передачи энергии возбуждения третьей частице пропорциональна концентрации таких частиц и зависит от их природы. Во всех случаях сечение прилипания электрона к атомам существенно меньше газокинетич. сечения, в отличие от сечений ионизации при образовании положит. И. в г.
Существенно большими сечениями обладают процессы образования отрицат. ионов многоатомных частиц. Это объясняется тем, что возбужденная многоатомная частица может быстро диссоциировать:
XY + e : [(XY-)]* : X + Y-
либо перераспределять энергию возбуждения по внутр. степеням свободы с образованием относительно долгоживущего состояния, способного стабилизироваться в столкновениях:
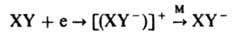
(М - третья частица). В последнем случае наблюдаются исключительно большие сечения в узком диапазоне энергий Ее. Так, сечение прилипания электронов к SF6 имеет чрезвычайно узкий максимум при энергиях электронов порядка kТ, равный 1,4.10-14 см2 (k - постоянная Больцмана, T - абс. т-ра).
При достаточно больших значениях Ее возможна т. наз. полярная диссоциация молекул без захвата электрона: XY + e : X+ + Y- +е.
Фотоионизация происходит с определенной вероятностью, когда фотон взаимод. с молекулой или атомом и энергия фотона Ehv равна или превышает потенциал ионизации молекулы или атома: А + hn : A+ + е. Зависимость сечения процесса от энергии Ehv, в отличие от ионизации электронным ударом, имеет резкие максимумы при Ehv = Ii, где Ii (i = 1, 2, ...) - первый, второй и т.д. потенциалы ионизации атома или молекулы. При Ehv>I1 возможны также диссоциативная фотоионизация с образованием двухзарядных ионов: А + hn : А2+ + 2е. Образование двухзарядных ионов обычно имеет место при выбивании "первичного" электрона из внутренней, напр., K-оболочки атома и переходе электрона из расположенной выше по энергии L-оболочки, что сопровождается испусканием рентгеновского кванта или "вторичного" электрона (Оже-электрона; см. Рентгеновская спектроскопия
). Фотоионизация возможна и при Ehv << I; в этом случае она носит многоступенчатый (многофотонный) характер (см. Многофотонные процессы
).
Ионизация при соударениях тяжелых частиц. Зависимость сечения процессов типа А + В : А + В+ + е; А+ + В : А+ + В+ + е от энергии Е относит. движения частиц А и В имеет такой же характер, как и при ионизации электронным ударом. Однако энергетич. масштаб существенно иной: сечение ионизации достигает максимума в области энергий порядка десятков кэВ и остается большим до энергий ~ 1 МэВ. Как и при электронном ударе, в максимуме зависимости сечение ионизации s(E) сравнимо с газокинетич. сечением соударения, а скорость относит. движения частиц сравнима со скоростью орбитального движения электронов в атоме или молекуле. Ионизация может происходить и за счет энергии возбуждения сталкивающихся частиц либо энергии хим. р-ции. Примером является ионизация Пеннинга А+ + В : А + В+ + е с участием возбужденных частиц А*, энергия к-рых превышает потенциал ионизации частиц В. Энергия хим. р-ции может эффективно приводить к ионизации
частиц продуктов, напр., в пламенах СН + О : СНО+ + е; N + О : NO+ + е. В результате тепловой эффект таких р-ций близок к нулю (для первой из приведенных р-ций) или существенно снижается (для второй р-ции он составляет + 2,75 эВ). Для р-ций типа К + Сl : К+ + Сl- тепловой эффект равен разности потенциала ионизации и сродства к электрону электроотрицат. частицы; для приведенной р-ции это всего лишь +0,72 эВ. Заметный вклад в снижение теплового эффекта р-ций может вносить и сродство к протону (к-рое для NH3, напр., составляет 9,4 эВ), а также энергия связи других ионов, образующих утяжеленные или кластерные ионы (напр., О2+ .О2, Аr+ .Аr).
Рекомбинация И. в г. Процессы типа А+ + В- либо АВ+ + е : А + В в общем случае протекают со скоростью, характерной для бимолекулярных р-ций и определяемой выражением:
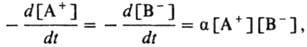
где t - время, [А+] и [В-] - концентрации положит. и отрицат. ионов (в см-3), a - т. наз. коэф. рекомбинации (в см3.с-1). Величина a меняется в широких пределах (от 10-6 до 10-14) в зависимости от характера процесса и природы участвующих в нем частиц. Наиб. медленной является радиац. рекомбинация, при к-рой энергия рекомбинации превращ. в энергию фотонов. В таких процессах участвуют, как правило, разноименно заряженные атомарные ионы А+ и В- либо атомарный ион и электрон: А+ + е : А + В + hn. Радиац. рекомбинация тепловых частиц (с энергией порядка kТ) и электронов происходит очень медленно, a < 10-14 см3.с-1. С существенно большими значениями a протекает рекомбинация с участием разноименно заряженных атомарных ионов (нейтрализация), приводящая к образованию нейтральных атомов в возбужденных состояниях. Так, для р-ции Н+ + Н- : Н* + Н макс. значение a достигается при образовании возбужденного атома Н* с главным квантовым числом п = 3 (a3 = 1,3.10-7см3.с-1 при 250 К).
Еще более распространена диссоциативная рекомбинация, в к-рой участвуют двухатомные и многоатомные ионы, включая ионные кластеры. Процессы этого типа обладают наиб. высокими значениями а, лежащими в области 10-8-10-6 см3.с-1. Механизм диссоциативной рекомбинации двухатомной молекулы можно представить последовательностью процессов: Х2+ + е : (X2*) : X* + X + кинетич. энергия. При захвате электрона положит. ионом образуется возбужденная молекула X2*, распадающаяся с образованием атомов в возбужденном и основном состояниях, к-рые обладают избыточной кинетич. энергией ("горячие" атомы). Поскольку переход X2* : X* + X происходит очень быстро (за время одного колебания, равное ~ 10-13 с), вероятность диссоциативной рекомбинации по порядку величины близка к единице, а a ~ 10-8-10-7 см3.с-1. Типичный пример диссоциативной рекомбинации двухатомных ионов:
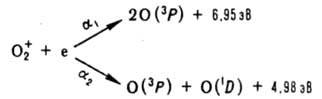
При комнатной т-ре a1 = 3.10-8, a2 = 1,7.10-7 см3.c-1.
Для рекомбинации с участием многоатомных ионов и, в частности, ионных кластеров a могут иметь значения ~ 10-6 см3.с-1. Так, рекомбинация кластеров Н3О+ .(Н2О)5 + е : продукты, происходящая при "т-ре" заряженных частиц 205 К, характеризуется a = (5-10).10-6 см3.с-1. Важная особенность рекомбинации с участием ионных кластеров - рост a с увеличением числа молекул в кластере.
Описанные процессы рекомбинации имеют место при невысоких давлениях (не более неск. сотен Па). Их вероятность обусловлена эффективностью способов отбора
избыточной энергии, выделяющейся при рекомбинации. Поэтому если у частицы появляются дополнит. возможности отдать избыточную энергию, вероятность рекомбинации возрастает. Такие условия возникают при повыш. давлениях, когда в пределах сферы взаимного притяжения зарядов ускоряющиеся ионы могут сталкиваться с нейтральными частицами и передавать им часть энергии.
При больших давлениях (атмосферном и выше) коэф. рекомбинации разноименно заряженных ионов м. б. выражен через их подвижности m+ и m-: a = 4pе(m+ + m-), что подтверждается эксперим. значениями a ~ 10-6 см3.с-1. При низких концентрациях ионов и низких давлениях повышается вероятность рекомбинации зарядов на стенке сосуда. Если длина своб. пробега иона больше или соизмерима с размерами сосуда, время жизни иона в отсутствие электрич. и магнитного полей определяется только временем его пробега между стенками. При меньших длинах своб. пробега время жизни tд ~ x2/2D, где х - расстояние между стенками, D - козф. диффузии. Если концентрации положит. и отрицат. ионов (или электронов) одинаковы, их диффузия происходит с одинаковой скоростью (т. наз. амбиполярная диффузия). Коэф. амбиполярной диффузии определяется средним значением подвижности диффундирующих частиц: D = (RT/e)m, где m = m+m-/m+ + m-, R - газовая постоянная.
Знание скоростей образования и гибели заряженных частиц позволяет определить их стационарную концентрацию в системе. В случае гомогенной квадратичной гибели по р-ции А+ + В- : продукты стационарные концентрации [А+] и [В-] равны 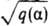 ; в случае диффузионной гибели на стенке они равны qtд, где q - скорость ионизации (в см-3.с-1). ; в случае диффузионной гибели на стенке они равны qtд, где q - скорость ионизации (в см-3.с-1).
Роль ионов в различных процессах. Важная роль И. в г. в радиац. химии обусловлена их высоким радиац. выходом, равным 3-4 парам ионов на 100 эВ поглощенной энергии, и участием в разл. ионно-молекулярных реакциях
, к-рые характеризуются большими скоростями и при не слишком больших мощностях дозы излучения успевают пройти прежде, чем произойдет рекомбинация. Так, при мощностях дозы 1016 эВ.см-3.с-1, типичных для газофазного радиолиза, время жизни иона до рекомбинации tn ~ 6.10-5с, тогда как характерное время р-ции А+ + В : продукты при [В] = 2,5.1019 см-3 ti ~ 4.10-10с. Величины tr и ti становятся равными при уменьшении [В] на 5 порядков либо при увеличении мощности дозы на 10 порядков. Поэтому практически любые радиационно-хим. процессы с участием ионов протекают в такой последовательности: ионизация - ионно-молекулярная р-ция - рекомбинация (причем в рекомбинации принимают участие не только вторичные ионы, но и ионы более глубоких поколений). Образовавшиеся при рекомбинации активные частицы (радикалы, атомы, возбужденные частицы) в свою очередь участвуют в хим. превращениях, давая конечные продукты радиолиза. Основными ионно-молекулярными р-циями в радиац. химии газов являются переход тяжелой частицы (протона) и перезарядка (недиссоциативная или диссоциативная).
При фотохим. р-циях И. в г. могут играть заметную роль только в далекой (коротковолновой) УФ области (см., напр., описанные ниже ионные процессы в земной атмосфере). В плазме электрич. разряда участие И. в г. в хим. р-циях незначительно, т.к., напр., в плазмохим. реакторах т-ра электронов составляет 103-2.104 К, что соответствует энергии Еe 0,1-2 эВ. Такая энергия достаточна для возбуждения молекул либо их диссоциации, но ионизировать газ способна лишь очень малая доля электронов. Напр., в тлеющем разряде в водороде при давлении 10-100 Па и плотности тока 10-1 А.см2 концентрация атомов Н м. б. доведена почти до 100%, а степень ионизации при этом будет менее 1%. В несамостоят. электрич. разрядах, где ионизация газа осуществляется внеш. источником, процессы с участием И. в г. могут играть практически такую же роль, что и в радиационно-хим. превращениях.
При высоких т-рах в условиях термодинамич. равновесия степень ионизации газа приближенно определяется ф-лой Саха:
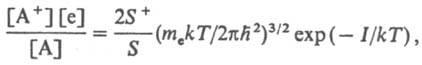
где [А+], [е], [А] - концентрации соответствующих частиц, S+ и S - статистич. веса А+ и А, тe - масса электрона, I - потенциал ионизации нейтральной частицы в основном состоянии. В пламенах могут наблюдаться сверхравновесные концентрации заряженных частиц порядка 1010-1011 см-3. Степень ионизации пламени и его электрич. проводимость м. б. повышены введением частиц с малым потенциалом ионизации либо частиц, ионизация к-рых облегчается за счет энергии хим. р-ции. Так, добавки щелочных металлов используются, напр., в магнитогидродинамич. преобразователях тепловой энергии в электрическую.
Высокий разогрев и вызванная им сильная ионизация воздуха возникают при прохождении через атмосферу метеорных тел, ракет и спутников.
Ионы в атмосфере Земли и Солнца. В разных слоях земной атмосферы ионизация обусловлена действием источников разной мощности: в приземном слое - это излучение радиоактивных изотопов земной коры, в тропосфере и нижней стратосфере (0-25 км) - космич. лучи, в ионосфере (65-600 км) - коротковолновое УФ излучение Солнца. Наиб. вклад в ионизацию земной атмосферы вносит поток УФ излучения с длинами волн короче 103 нм, к-рый поглощается на высотах 100-300 км, ионизируя в осн. О, N2, O2. На высоте ~ 300 км абс. максимум дневной концентрации заряженных частиц (гл. обр. О+ и е) составляет ~ 106 см-3. Концентрация электронов здесь зависит от скорости ионно-молекулярных р-ций, превращающих атомарные ионы О+, практически нерекомбинирующие, в быстро рекомбинирующие молекулярные ионы O2+ и NO+: О+ + O2 : O2+ + O; О+ + N2 : NO+ + N. На высотах 100-150 км преобладают ионы NO+ и О2+, а ниже 90 км начинается образование ионных кластеров и отрицат. ионов, так что на высотах ниже 65-70 км днем электроны практически отсутствуют.
Процессы с участием заряженных частиц определяют не только состав и концентрацию ионов, но оказывают заметное влияние на содержание нейтральных активных частиц в атмосфере. Так, изменение скорости образования ионов в стратосфере приводит к изменению скорости образования оксидов азота, разрушающих стратосферный озон. На высотах 80-90 км ионизация О2 и р-ция О2+ с Н2О приводят к образованию Н и ОН. При рекомбинации мол. ионов в ионосфере рождаются возбужденные и невозбужденные "горячие" атомы (обладающие избыточной кинетич. энергией).
Важным процессом в солнечной атмосфере с участием ионов является образование непрерывного солнечного спектра излучения в видимой области. Это излучение испускается при поглощении фотонов, поступающих из внутр. слоев Солнца, ионами Н- (сродство к электрону 0,755 эВ).
Лит.: Смирнов Б. М., Ионы и возбужденные атомы в плазме, М., 1974; Месси Г., Отрицательные ионы, пер. с англ., М., 1979; Брасье Г., Соломон С., Аэрономия средней атмосферы, пер. с англ., Л., 1987.
И. К. Ларин, В. Л. Тальрозе.
|


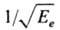 . Вероятность Wt передачи энергии возбуждения третьей частице пропорциональна концентрации таких частиц и зависит от их природы. Во всех случаях сечение прилипания электрона к атомам существенно меньше газокинетич. сечения, в отличие от сечений ионизации при образовании положит. И. в г.
Существенно большими сечениями обладают процессы образования отрицат. ионов многоатомных частиц. Это объясняется тем, что возбужденная многоатомная частица может быстро диссоциировать:
. Вероятность Wt передачи энергии возбуждения третьей частице пропорциональна концентрации таких частиц и зависит от их природы. Во всех случаях сечение прилипания электрона к атомам существенно меньше газокинетич. сечения, в отличие от сечений ионизации при образовании положит. И. в г.
Существенно большими сечениями обладают процессы образования отрицат. ионов многоатомных частиц. Это объясняется тем, что возбужденная многоатомная частица может быстро диссоциировать:
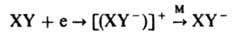
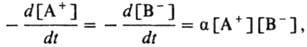

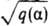 ; в случае диффузионной гибели на стенке они равны qtд, где q - скорость ионизации (в см-3.с-1).
; в случае диффузионной гибели на стенке они равны qtд, где q - скорость ионизации (в см-3.с-1).