Химическая энциклопедия
"ЖЕЛЕЗА ОКСИДЫ"
Главная - Химическая энциклопедия - буква Ж - ЖЕЛЕЗА ОКСИДЫ
ЖЕЛЕЗА ОКСИДЫ
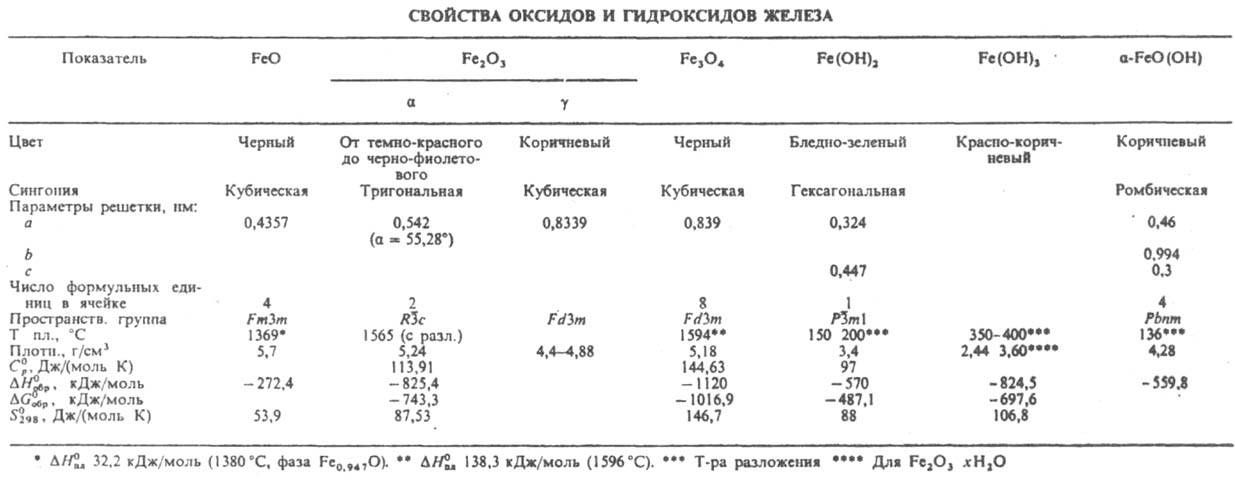
. Оксид FeO (в технике - вюстит). В кристаллич. решетке вюстита имеются вакантные узлы, и его состав отвечает ф-ле FexO, где х = 0,89-0,95; ур-ние температурной зависимости давления разложения: lg p(O2, в мм рт. ст.) = - 26730/T+ 6,43 (T > 1813 К); см. также табл. В воде практически не раств., хорошо раств. в к-тах, р-рах щелочей. Легко окисляется; пирофорeн. После прокаливания хим. активность и пирофорность FeO снижаются.
В природе - чрезвычайно редкий минерал иоцит. Получают восстановлением Fe2O3 водородом либо СО или при прокаливании в атмосфере N2 2FeC2O4.3H2O.
Сесквиоксид Fe2O3 существует в трех полиморфных модификациях: наиб. устойчивая а (минерал гематит), g (маггемит, оксимагнетит) и d (с тригональной кристаллич. решеткой); т-ры перехода a : g 677°С, g : d 777°С; DH0 перехода a : g 0,67 кДж/моль. Для модификации a-Fe2O3 ур-ние температурной зависимости давления разложения: lg p(O2, в мм рт. ст.) = - 10291/T+ 5,751gT - 1,09.10-3Т -0,75.105Т-2 - 12,33; раств. в соляной и серной к-тах, слабо - в HNO3; парамагнетик, точка Нееля 953 К. Модификации g- и d-Fe2O3 ферримагнитны; g-Fе2О3образуется при низкотемпературном окислении Fe3O4 и Fe, d-Fe2O3 м. б. получен при гидролизе и окислении р-ров солей Fe(II).
Оксид Fe(II,III) - соед. ф-лы Fe3O4, или FeO.Fe2O3, FeII(FeIIIO2)2 (минерал магнетит), при нагр. разлагается; при 627 °С a-форма переходит в b; ур-ние температурной зависимости давления разложения: lgp(O2, в мм рт. ст.) = = - 33265/Т+ 13,37 (Т > 843 К); ферримагнетик, точка Кюри 900 К; отличается высокой электрич. проводимостью. Раств. в к-тах с образованием солей Fe(II) и Fe(III), прокаленный при 1200-1300 °С прир. магнетит практически не раств. в к-тах и их смесях. При нагр. на воздухе окисляется до Fe2O3. Получают действием водяного пара на раскаленное железо, восстановлением Fe2O3, окислением FeO.
Ж. о. соответствует ряд гидроксидов. Гидроксид Fe(OH)2 образуется при действии щелочи на водные р-ры солей Fe(II); быстро окисляется до FeO(OH). Р-римость в воде 0,00015 г в 100 г (18°С), раств. в к-тах, р-рах щелочей с образованием гидроксоферратов(II), напр. Na2[Fe(OH)4], и р-рах NH4Cl.
Гидроксиды Fe(III) образуют в природе ряд бурых железняков: гидрогематит Fe2O3.0,1H2O (твердый р-р воды в гематите), турьит 2Fe2O3.Н2О (тонкая мех. смесь гётита и гидрогематита), гётит a-FeO(OH), или Fe2O3.H2O, лепидокрокит g-FeO(OH), гидрогётит 3Fe2O3.4H2O, лимонит 2Fe2O3.3H2O, ксантосидерит Fe2O3.2H2O и лимнит Fe2O3.3H2O (твердые р-ры воды в гётите ).
|
Поделитесь с друзьями:
Вы можете поставить ссылку на это слово:
будет выглядеть так: ЖЕЛЕЗА ОКСИДЫ
будет выглядеть так: Что такое ЖЕЛЕЗА ОКСИДЫ