Химическая энциклопедия
"ИЗОТОПНЫЙ ОБМЕН"
Главная - Химическая энциклопедия - буква И - ИЗОТОПНЫЙ ОБМЕН
ИЗОТОПНЫЙ ОБМЕН
, самопроизвольное перераспределение изотопов хим. элемента между разл. фазами системы (в частности, между разл. агрегатными состояниями одного и того же в-ва), частицами (молекулами, ионами) или внутри молекул (сложных ионов). В И. о. могут участвовать как стабильные, так и радиоактивные нуклиды. При И. о. сохраняется неизменным элементный состав каждого участвующего в обмене в-ва, изменяется лишь его изотопный состав. Если обменивающиеся изотопами молекулы, ионы и т. п. находятся в одной фазе, И. о. наз. гомогенным, если в разных фазах - гетерогенным. Так, при гомогенном И. о. с участием молекул воды 1Н1НО и DDO образуются молекулы HDO; при гетерог. И. о. между парами иода, меченного радионуклидом 131I, и кристаллич. иодом радиоактивные атомы переходят из пара в кристаллы. В результате И. о. изотопный состав всех форм выравнивается и устанавливается равномерное распределение изотопов (равнораспределение).
И. о. можно рассматривать как обычную хим. р-цию, в к-рой исходные в-ва и продукты различаются изотопным составом. Внутр. энергия системы при этом практически не изменяется (нулевые частоты колебаний молекул, обменивающихся изотопами, почти одинаковы) и тепловой эффект Q = 0. Последнее означает, что для прямого и обратного И. о. энергии активации равны; кроме того, константы равновесия К практически не зависят от т-ры. Если в И. о. участвуют легкие элементы, становятся заметными изотопные эффекты
, вследствие чего константы равновесия могут существенно отличаться от 1.
Чем ближе система, в к-рой протекает И. о., к состоянию равнораспределения, тем больше число вариантов распределения изотопов в системе, т. е. выше число микросостояний, через к-рое м. б. реализована система. Т. обр., при И. о. энтропия системы растет; максимум энтропии достигается при равнораспределении.
Скорость И. о. во многом зависит от его механизма. В частности, гомог. И. о. может протекать по диссоциативному или ассрциативному механизму, м. б. связан с переносом электрона или с перемещением групп атомов. Напр., обмен радиоактивным иодом между кристаллами AgI и
р-ром, содержащим -ln(1 - F) = (ln2/t1/2)t, к-рое позволяет по эксперим. значениям F определить t1/2 и рассчитать константу скорости И. о. Напр., для бимолекулярного И. о. (р-ция второго порядка) константа скорости k равна: k = (ln 2/t1/2)[1/(a + b)], где а и b - молярные концентрации обменивающихся форм. Определив значения k при разных т-рах, можно на основании ур-ния Аррениуса найти энергию активации И. о., что позволяет, в частности, судить о прочности связи атомов, участвующих в И. о. Скорость гетерог. И. о. зависит как от скорости подвода и отвода обменивающихся атомов от пов-сти раздела фаз, так и непосредственно от скорости самого И. о. Если в И. о. участвует твердая фаза, то при достаточно интенсивном перемешивании паровой или жидкой фаз скорость всего процесса определяется скоростью диффузии обменивающегося атома от границы раздела фаз вовнутрь твердой фазы. И. о. используют при изотопов разделении , получении меченых соединений ; с его помощью изучают строение молекул. На анализе И. о. основан один из способов определения низких давлений насыщенных паров. В отд. случаях И. о. может исказить результаты опыта; так, при изучении И. о. между в-вами, растворенными в воде, нужно учитывать возможность обмена изотопов водорода между исследуемыми в-вами и молекулами воды. Лит.: Несмеянов А. Н., Радиохимия. 2 изд., М., 1978, Радиоактивные индикаторы в химии. Основы метода, под ред. В. Б. Лукьянова. 3 изд., М., 1985. С. С. Бердоносов.
|
Поделитесь с друзьями:
Вы можете поставить ссылку на это слово:
будет выглядеть так: ИЗОТОПНЫЙ ОБМЕН
будет выглядеть так: Что такое ИЗОТОПНЫЙ ОБМЕН
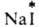 (здесь и далее знак * указывает радиоактивный атом), протекает в результате диссоциации
(здесь и далее знак * указывает радиоактивный атом), протекает в результате диссоциации 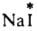 и AgI в р-ре. Обмен хлором между газообразным
и AgI в р-ре. Обмен хлором между газообразным 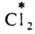 и парами FeCl3 также определяется диссоциацией FeCl3 при нагр. с образованием FeCl2 и атома Сl:
и парами FeCl3 также определяется диссоциацией FeCl3 при нагр. с образованием FeCl2 и атома Сl:
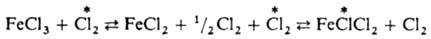
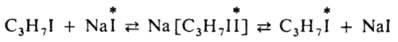
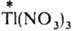 :
:

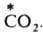 и твердым ВаСО3:
и твердым ВаСО3: