Химическая энциклопедия
"ФУНКЦИИ КИСЛОТНОСТИ"
Главная - Химическая энциклопедия - буква Ф - ФУНКЦИИ КИСЛОТНОСТИ
ФУНКЦИИ КИСЛОТНОСТИ
,
определяют протонирую-щую способность р-ров к-т. Если протонируется нейтральная
молекула В, Ф. к. обозначают H0, если анион или катион - H_
или H+ соотв. Ф. к. характеризуют равновесие протонирова-ния
в зависимости от концентрации к-ты и позволяют рассчитывать степени протонирования
реагентов в хим. р-ции, ионизирующихся по тому же механизму, что и применяемые
для измерений Ф. к. стабильные соед. (индикаторы). Ф.к. H0 отвечает
условно записанному равновесию BH+ где аB,
aH+ и аBH+ - термодинамич. активности соотв.
основания В, протона H+ и протонир. формы BH+; с - их равновесные
концентрации; f- коэф. активности. Соотношение Аналогично измеряют Н_ и H+,.исходя из след, ур-ний: Для определения Ф. к. обычно
используют индикаторный метод, при этом необходимо знать константу основности
индикатора и отношение концентраций его непротонир. и протонир. форм (измеряется
спектрофотометрически или др. методом). Посредством одного индикатора можно
измерить H0 в пределах 2-3 единиц ее изменения, в более
широких диапазонах кислотностей применяют серии индикаторов. Для установления
шкалы кислотности используют в осн. производные нитроанилина. За стандартное состояние
для шкалы кислотности берут бесконечно разб. водный р-р сильной к-ты, где коэф.
активности fB и fBH+ принимаются равными
единице, а активность протонов равной их концентрации. В таких р-рах H0
численно равна рН. Индикаторный метод измерения
H0 состоит в следующем. Сначала выбирают наиб. сильное
основание В, к-рое практически полностью протонируется в очень разб. р-рах к-ты
НА. Измерив отношение сB/сBH+, из зависимости lg (сB/сBH+)
от моляльной концентрации МНА к-ты определяют Численные значения Ф.к.
связаны с силой к-ты. Так, 100%-ная H2SO4 имеет H0
= -11,94, чистая CH3SO3H-H0 = -7,86. Ф. к., судя по нек-рым
данным, мало зависят от т-ры. Однако при повышении т-ры могут изменяться Ф. к. описывают только
процесс протонирования. Во мн. случаях, кроме этого процесса, ионизация основания
может заключаться также в образовании ионных пар, разл. комплексов протонир.
формы с молекулами р-рителя, димеров и т.д. В таких случаях для корректного
использования Ф.к. при описании ионизации слабого основания необходимо знать
механизм его ионизации и измерять равновесные концентрации всех образующихся
форм основания В. На практике обычно измеряют равновесную концентрацию только
одной формы (обычно - неионизированной), а концентрацию формы BH+
вычисляют из ур-ния баланса концентраций, тем самым постулируя простой механизм
протонирования. Такая практика, а также недоказанность постулата Гаммета привели
к появлению ряда Ф.к., относящихся к разл. классам хим. соед. (HА
- Ф. к. амидов, Развивая этот подход, P.
Кокс и К. Эйтс (1978) ввели понятие "избыточная кислотность" X,
к-рая отражает разность между наблюдаемой (формально измеренной) Ф. к. для данного
класса соед. и "идеальной" Ф.к., строго подчиняющейся постулату
Гаммета (H0 , Н_). Отклонения от соблюдения постулата
Гаммета выражаются ур-нием: где В* - "идеальное"
основание; В - основание из данного ряда; m* - параметр, характерный
для данного класса соед. Практическое применение избыточной кислотности X основано на линейном соотношении: где CH+
- равновесная концентрация протонов в р-ре. Схема протонирования слабого
основания (В + H+ где Дигидрат протона Корректное использование
Ф.к. для расчетов степеней протонирования и констант основности хим. соед. в
р-рах к-т должно быть основано, во-первых, на установлении механизма ионизации
данного соед., во-вторых, на уверенности в том, что образующаяся протонир. форма
есть ион, образованный сильной симметричной водородной связью. Понятие Ф.к. введено Л.
Гамметом в 1932. Лит.: Гаммет Л.
П., Основы физической органической химии, пер. с англ., M., 1972; Либрович H.Б.,
"Изв. АН СССР. Сер. хим.", 1990, № 1, с. 32-35; Rochester C.H.,
Acidity functions, L.-N. Y., 1970; Cox R. А., Yates K., "J. Amer.
Chem. Soc.", 1978, v. 100, № 12, p. 3861-67. H. Б. Либрович. |
Поделитесь с друзьями:
Вы можете поставить ссылку на это слово:
будет выглядеть так: ФУНКЦИИ КИСЛОТНОСТИ
будет выглядеть так: Что такое ФУНКЦИИ КИСЛОТНОСТИ
 В + H+, где BH+ - протонир. форма основания В. Константа
равновесия этого процесса
В + H+, где BH+ - протонир. форма основания В. Константа
равновесия этого процесса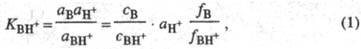
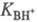 наз. константой основности соед. В.
наз. константой основности соед. В.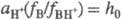 наз. кислотностью среды. Ф-ция кислотности H0 = -lg h0
- При логарифмировании выражения (1) получим соотношение
наз. кислотностью среды. Ф-ция кислотности H0 = -lg h0
- При логарифмировании выражения (1) получим соотношение 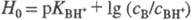 ,
где
,
где 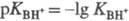 . При
измерении Ф. к. исходят из предположения, что в концентрир. водных р-рах сильных
к-т изменение отношения
. При
измерении Ф. к. исходят из предположения, что в концентрир. водных р-рах сильных
к-т изменение отношения 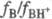 не зависит от хим. природы основания-индикатора В (постулат Гаммета).
не зависит от хим. природы основания-индикатора В (постулат Гаммета).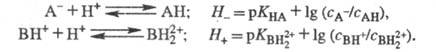
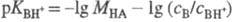 . В таких р-рах -lg МНА = рН, а соблюдение этой зависимости
подтверждает, что в данном интервале концентраций к-ты коэф. активности не изменяются.
Для определения Ф.к. более концентрир. р-ров выбирают след. индикатор таким
образом, чтобы, являясь более слабым основанием, он начинал протонироваться
в тех р-рах к-ты, где первый индикатор еще не полностью протонирован. В этом
"интервале перекрывания" определяют константу основности второго
индикатора D: рКBH+ - рКDH+ = = lg
(cD/cDH+) - Ig (сB/сBH+). Далее,
измеряя cD/cDH+ в более концентрир. р-рах к-ты и зная
pKDH+, определяют H0 для
этих р-ров. Затем аналогичную процедуру проводят со след. индикатором и т. д.
Таким образом, для измерения H0 необходима серия индикаторов.
Так, для системы HCl - H2O (до 16 M HCl) нужно 7-8 индикаторов, для
водных р-ров H2SO4 от разбавл. до 100% H2SO4
- 10-12 индикаторов.
. В таких р-рах -lg МНА = рН, а соблюдение этой зависимости
подтверждает, что в данном интервале концентраций к-ты коэф. активности не изменяются.
Для определения Ф.к. более концентрир. р-ров выбирают след. индикатор таким
образом, чтобы, являясь более слабым основанием, он начинал протонироваться
в тех р-рах к-ты, где первый индикатор еще не полностью протонирован. В этом
"интервале перекрывания" определяют константу основности второго
индикатора D: рКBH+ - рКDH+ = = lg
(cD/cDH+) - Ig (сB/сBH+). Далее,
измеряя cD/cDH+ в более концентрир. р-рах к-ты и зная
pKDH+, определяют H0 для
этих р-ров. Затем аналогичную процедуру проводят со след. индикатором и т. д.
Таким образом, для измерения H0 необходима серия индикаторов.
Так, для системы HCl - H2O (до 16 M HCl) нужно 7-8 индикаторов, для
водных р-ров H2SO4 от разбавл. до 100% H2SO4
- 10-12 индикаторов.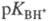 оснований.
оснований.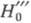 -
третичных аминов, HI -индолов, НB - бензофенонов,
НM - азуленов и т.д.). Нек-рые из
этих Ф. к. связаны с иным, чем протонирование, механизмом ионизации. Это м.
б. образование ионных пар типа BH+·A- (А- -
анион к-ты), к-рое имеет место наряду с протонированием (
-
третичных аминов, HI -индолов, НB - бензофенонов,
НM - азуленов и т.д.). Нек-рые из
этих Ф. к. связаны с иным, чем протонирование, механизмом ионизации. Это м.
б. образование ионных пар типа BH+·A- (А- -
анион к-ты), к-рое имеет место наряду с протонированием (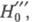 HI), либо образование комплекса B·HA (НM).
Возможны случаи, когда действительно не соблюдается постулат Гаммета.
HI), либо образование комплекса B·HA (НM).
Возможны случаи, когда действительно не соблюдается постулат Гаммета.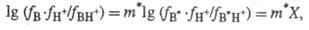
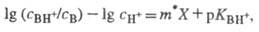
 BH+)
не есть реальное хим.
равновесие в р-рах к-т. Протон в таких р-рах существует в виде простейшего устойчивого
гидрата
BH+)
не есть реальное хим.
равновесие в р-рах к-т. Протон в таких р-рах существует в виде простейшего устойчивого
гидрата 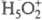 , а протонирование основания В есть р-ция замещения: В + H5O2+
, а протонирование основания В есть р-ция замещения: В + H5O2+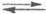 BHOH2+
+ H2O. Индикаторные отношения
BHOH2+
+ H2O. Индикаторные отношения 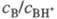 и константы основности вычисляют так же, как и при формальной схеме протонирования:
и константы основности вычисляют так же, как и при формальной схеме протонирования: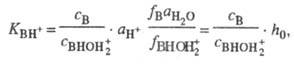
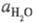 - активность воды. Присутствие
- активность воды. Присутствие 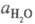 в ф-ле для кислотности
объясняет известный факт независимости отношения
в ф-ле для кислотности
объясняет известный факт независимости отношения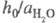 от природы сильной к-ты (для других Ф. к. это не
соблюдается).
от природы сильной к-ты (для других Ф. к. это не
соблюдается).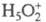 и протонир. форма.
и протонир. форма.  образованы
сильной симметричной водородной связью центр, протона: (Н2О...Н...ОН2)+
и (В...Н...ОН2)+. Геом. и энергетич. параметры этой связи
не зависят от структуры участвующих в ней частиц, а ее энергия разрыва достаточно
велика (134,1-142,5 кДж/моль). Этим можно объяснить соблюдение постулата Гаммета.
Отклонения от соблюдения постулата, в частности, м. б. объяснено образованием
другой протонир. формы по схеме: В + H5O2
образованы
сильной симметричной водородной связью центр, протона: (Н2О...Н...ОН2)+
и (В...Н...ОН2)+. Геом. и энергетич. параметры этой связи
не зависят от структуры участвующих в ней частиц, а ее энергия разрыва достаточно
велика (134,1-142,5 кДж/моль). Этим можно объяснить соблюдение постулата Гаммета.
Отклонения от соблюдения постулата, в частности, м. б. объяснено образованием
другой протонир. формы по схеме: В + H5O2 BH+
+ 2H2O. Такие случаи имеют место, если разность сродства к протону
молекул В и H2O превышает 113 кДж/моль.
BH+
+ 2H2O. Такие случаи имеют место, если разность сродства к протону
молекул В и H2O превышает 113 кДж/моль.