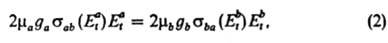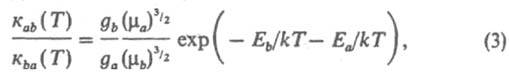Химическая энциклопедия
"ДЕТАЛЬНОГО РАВНОВЕСИЯ ПРИНЦИП"
Главная - Химическая энциклопедия - буква Д - ДЕТАЛЬНОГО РАВНОВЕСИЯ ПРИНЦИП
ДЕТАЛЬНОГО РАВНОВЕСИЯ ПРИНЦИП
в
химической кинетике, связывает кинетич. характеристики прямого и обратного микроскопич. процессов (квантового перехода или элементарной хим. р-ции), происходящих при соударениях частиц (атомов, молекул). В рамках динамич. описания системы взаимодействующих частиц, при к-ром вероятность процесса определяется энергией каждой частицы, изменение энергии при соударениях характеризуется сечением перехода или сечением р-ции (см. Столкновений теория
). Переходы частицы из начального квантового состояния а в конечное b и обратно происходят при определенных значениях энергии относит. движения частиц (соотв. Eat и Ebt). Внутр. энергия частицы в обоих рассматриваемых состояниях (соотв. Еа и Eb) связана с Eat и Ebt законом сохранения:
к/к = К(Т). (4) В форме (4) Д. р. п. позволяет в отсутствие хим. равновесия рассчитывать константу скорости прямой р-ции по константе скорости обратной р-ции и известной константе равновесия. Часто при формулировке Д. р. п. принимают в качестве исходного предположение о равенстве скоростей прямого и обратного процессов при равновесии и получают соотношение типа (3). Однако при таком подходе остается нераскрытым смысл Д. р. п. на динамич. уровне рассмотрения системы. Между тем для неравновесных р-ций, когда нельзя однозначно определить т-ру системы, Д. р. п. может быть использован только в виде соотношения типа (2). Лит. см. при статьях Динамика элементарного акта , Неравновесная химическая кинетика . Е. Е. Никитин.
|
Поделитесь с друзьями:
Вы можете поставить ссылку на это слово:
будет выглядеть так: ДЕТАЛЬНОГО РАВНОВЕСИЯ ПРИНЦИП
будет выглядеть так: Что такое ДЕТАЛЬНОГО РАВНОВЕСИЯ ПРИНЦИП
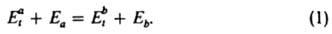
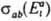 и
и 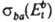 прямого и обратного переходов:
прямого и обратного переходов: